
1月21日,由濱州市人民醫(yī)院腫瘤科作為分中心承接的國際多中心藥物臨床試驗(yàn)“JS004-008-III-SCLC: 特瑞普利單抗聯(lián)合或不聯(lián)合Tifcemalimab(JS004/TAB004)作為局限期小細(xì)胞肺癌放化療后未進(jìn)展患者的鞏固治療的隨機(jī)�����、雙盲���、安慰劑對(duì)照�����、全球多中心III期臨床研究”啟動(dòng)會(huì)順利召開�����。該臨床試驗(yàn)由山東省腫瘤醫(yī)院-于金明院士作為Leading PI���,計(jì)劃在全球210個(gè)研究中心開展�����,共納入756例受試者����,我院腫瘤科作為分中心參與其中����。

濱州市人民醫(yī)院副院長于洪建、機(jī)構(gòu)辦主任于鋒英�、腫瘤科PI楊煥蓮、機(jī)構(gòu)辦成員��、腫瘤科研究團(tuán)隊(duì)����、呼吸內(nèi)科成員���、影像科室以及申辦方、CRO/SMO公司代表等參加此次會(huì)議����,會(huì)議由GCP腫瘤專業(yè)PI楊煥蓮主任主持。
啟動(dòng)會(huì)上����,于洪建副院長表示,我院對(duì)臨床試驗(yàn)工作一直以來都高度重視��,臨床試驗(yàn)對(duì)于醫(yī)院的發(fā)展�、學(xué)科的建設(shè)具有積極的推動(dòng)意義。此次承接的全球多中心III期臨床試驗(yàn)����,更是具有里程碑式的意義����,期待借助臨床試驗(yàn)平臺(tái)培養(yǎng)更多優(yōu)秀的研究型人才,推動(dòng)學(xué)科建設(shè)與發(fā)展��,不斷提升醫(yī)院的臨床科研能力及綜合實(shí)力。申辦方CRA對(duì)本項(xiàng)目研究背景���、臨床研究方案�����、毒性和不良反應(yīng)管理等方面進(jìn)行詳細(xì)介紹���,并與研究團(tuán)隊(duì)討論研究細(xì)節(jié)和互動(dòng)答疑。
在會(huì)議總結(jié)中�,機(jī)構(gòu)辦于鋒英主任再次強(qiáng)調(diào)對(duì)于符合入組條件的患者積極入組,同時(shí)強(qiáng)調(diào)藥物臨床試驗(yàn)質(zhì)量的重要性���,要求每位研究者必須認(rèn)真研讀并遵守試驗(yàn)方案�,保證數(shù)據(jù)真實(shí)���、嚴(yán)謹(jǐn)����、可追溯�����,各參與方要高度重視、明確職責(zé)���、緊密配合��,保障患者權(quán)利和安全�,保證臨床試驗(yàn)質(zhì)量����。
本次啟動(dòng)會(huì)的成功召開,標(biāo)志著我院腫瘤藥物臨床試驗(yàn)工作邁上新臺(tái)階�����,將為臨床研究注入新的活力�,進(jìn)一步推動(dòng)學(xué)科的建設(shè)與發(fā)展。未來�����,腫瘤科將繼續(xù)大力推進(jìn)藥物臨床試驗(yàn)工作����,不斷提升臨床試驗(yàn)研究能力���、助力腫瘤醫(yī)療�、科研高質(zhì)量發(fā)展,更好地服務(wù)于受試者�,服務(wù)于社會(huì),為腫瘤患者提供更多更有效的治療方案�。
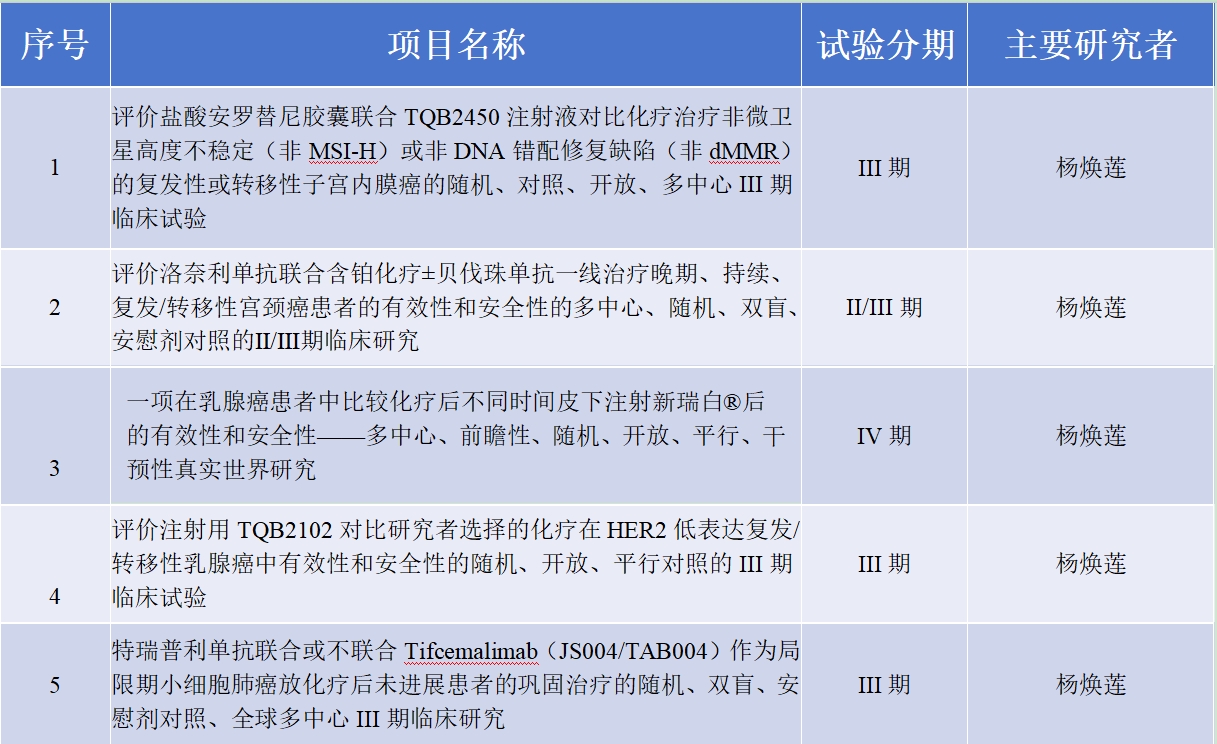
濱州市人民醫(yī)院腫瘤專業(yè)GCP資質(zhì)自2024年1月成功備案以來,已順利承接4項(xiàng)III期注冊(cè)類藥物臨床試驗(yàn)���,1項(xiàng)IV期改寫藥物適應(yīng)癥的藥物臨床試驗(yàn)�。
(腫瘤科一病區(qū) 張瑩瑩)